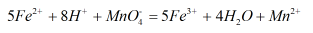铁与酸性高锰酸钾能能发生反应吗
10Fe+6KMnO4+24H2SO4===5Fe2(SO4)3+3K2SO4+6MnSO4+24H2O(酸性条件下)、高锰酸钾有强氧化性,铁有还原性,加热条件下会发生氧化还原反应,铁会被氧化成正三价, 锰会还原成正四价,离子方程式为5Fe+3MnO4-+24H+===5Fe3++3Mn2++12H2O。
一般可以认为高锰酸钾和铁固体不反应。
将高锰酸钾和铁屑混合(固体),经过试验观察,无任何反应。如果是高锰酸钾溶液(不加热)会很缓慢的反应,要几天才能观察到现象。中学阶段可认为不反应。
1毫升高锰酸钾相当于多少的铁什么意思
(1).在上述反应中(
fe
)元素被氧化,---------------因为fe元素的化合价升高,从fe(no3)3中的+3价,升高到na2feo4中的+6价
当3molcl2参与反应时,转移电子的总数为(
6mol
)-----------因为每个cl得到1个电子,3molcl2即得到6mol电子,或者每个fe失去3个电子,2molfe(no3)3即失去6mol电子
(2).
铁酸钠之所以能净水,除了能消毒外,另一个原因是(
在消毒反应中,na2feo4会生成fe3+,水解生成fe(oh)3胶体,具有较强的吸附作用,吸附水中的杂质而沉降,起到净水的作用
)
高锰酸钾与二价铁离子会发生什么反应
高锰酸钾能够将二价铁离子氧化成三价铁离子,方程式为:
高锰酸钾,无机化合物,深紫色细长斜方柱状结晶,有金属光泽。
高锰酸钾具有强氧化性,在实验室中和工业上常用作氧化剂,遇乙醇即分解。在酸性介质中会缓慢分解成二氧化锰、钾盐和氧气。光对这种分解有催化作用,故在实验室里常存放在棕色瓶中。从元素电势图和自由能的氧化态图可看出,它具有极强的氧化性。在碱性溶液中,其氧化性不如在酸性中的强。
制备:
工业上制备KMnO4较为简便的方法是用铂作阴极电解氧化K2MnO4:首先用KOH将含60%MnO2的矿石转化为K2MnO4,再电解氧化生成KMnO4。
应用:
1、在化学品生产中,广泛用作为氧化剂;
2、在医药上用作防腐剂、消毒剂、除臭剂及解毒剂;
3、在水质净化及废水处理中,作水处理剂,以氧化硫化氢、酚、铁、锰和有机、无机等多种污染物,控制臭味和脱色;
4、在气体净化中,可除去痕量硫、砷、磷、硅烷、硼烷及硫化物;
5、在采矿冶金方面,用于从铜中分离钼,从锌和镉中除杂,以及化合物浮选的氧化剂;6、还用于作特殊织物、蜡、油脂及树脂的漂白剂,防毒面具的吸附剂,木材及铜的着色剂等。
高锰酸钾和铁会反应么
在一般条件下不会反应,需要一定的条件,加热时,会发生氧化还原反应,高锰酸钾有很强的氧化性,铁也有还原剂性。反应后铁会被氧化成正三阶, 锰会还原成正四阶,还有你好,K2MnO4是锰酸钾,高锰酸钾是KMnO4。
铁与高锰酸钾反应的化学方程式
KMnO4必须在酸性条件下才能与Fe反应
化学反应方程式10Fe+6KMnO4+24H2SO4===5Fe2(SO4)3+3K2SO4+6MnSO4+24H2O
离子反应方程式
5Fe+3MnO4-+24H+===5Fe3++3Mn2++12H2O
高锰酸钾和硫酸铁反应方程式
不会反应,但高锰酸钾会与硫酸亚铁反应
反应方程式如下
2KMnO4+10FeSO4+8H2SO4==K2SO4+5Fe2(SO4)3+2MnSO4+8H2O
高锰酸钾与铁反应生成氧化铁么详细些
这应该是在酸性条件下具有强氧化性可以将铁氧化成正三价,但不是氧化铁;
如果是在加热的条件下,则高锰酸钾分解生成的氧气可以与铁反应生成氧化铁。
铁与高锰酸钾反应方程式
高锰酸钾与铁在一般条件下不会反应,需要一定的条件,加热时,会发生氧化还原反应,高锰酸钾会褪色,Mn由+7价---+4价 ,Fe由+2---+3另外,MnO4-在酸性、中性、碱性的溶液中都可以把Fe从+2价氧化到+3价。 酸性: 5Fe2+ + MnO4- + 8H+ = 5Fe3+ + Mn2+ + 4H2O 中性: 9Fe2+ + 3MnO4- + 6H2O = 5Fe3+ + 3MnO2↓ + 4Fe(OH)3↓ 碱性: Fe2+ + MnO4- + 3OH- = Fe(OH)3↓ + MnO42- 一般都是用酸性的KMnO4溶液。
酸性高锰酸钾与硫酸铁反应的化学方程式怎样写
化学方程式:
2KMnO₄+10FeSO₄+8H₂SO₄==K₂SO₄+2MnSO₄+5Fe₂(SO₄)₃+8H₂O
高锰酸钾广泛用作为氧化剂,例如用作制糖精,维生素C、异烟肼及安息香酸的氧化剂;在医药上用作防腐剂、消毒剂、除臭剂及解毒剂;在水质净化及废水处理中,作水处理剂,以氧化硫化氢、酚、铁、锰和有机、无机等多种污染物,控制臭味和脱色。
(9)高猛酸铁扩展阅读:
高锰酸钾注意事项:
1、危险特性
强氧化剂。遇浓硫酸、铵盐能发生爆炸。遇甘油能引起自燃。与有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。
灭火方法: 采用水、雾状水灭火。
2、应急处理
隔离泄漏污染区,限制出入。建议应急处理人员戴防尘面具,穿防毒服。不要直接接触泄漏物。小量泄漏:用砂土、干燥石灰或苏打灰混合。用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏:收集回收或运至废物处理场所处置。
3、操作注意事项
密闭操作,加强通风。操作人员必须经过专门培训,严格遵守操作规程远离火种、热源,工作场所严禁吸烟、进食和饮水。
避免产生粉尘。避免与还原剂、活性金属粉末接触。搬运时要轻装轻卸,防止包装及容器损坏。配备相应品种和数量的消防器材及泄漏应急处理设备。倒空的容器可能残留有害物。
铁和高锰酸钾 反应方程式 条件
高锰酸钾必须在酸性条件下才能与铁反应。
化学反应方回程式:
10Fe+6KMnO4+24H2SO4===5Fe2(SO4)3+3K2SO4+6MnSO4+24H2O
离子反答应方程式:
5Fe+3MnO4-+24H+===5Fe3++3Mn2++12H2O
(10)高猛酸铁扩展阅读:
1、用高锰酸钾溶液滴定硫酸亚铁——自身指示剂。
2、MnO4- +5 Fe2+ + 8H+ == Mn2+ + 5Fe3+ + 4H2O
3、在稀溶液中滴定后生成的Mn2+颜色很浅,Fe3+颜色也不深。
4、滴定终点,最后半滴高锰酸钾溶液过量,溶液颜色发生突变,呈浅粉色,指示终点。
5、优点是终点变色敏锐,方便,终点误差小!